Αντισώματα AChR, MuSK και LRP4: Εξέταση για Μυασθένεια Gravis
Σύντομη περίληψη:
Τα αντισώματα AChR είναι η βασική εξέταση αίματος για τη διερεύνηση της Μυασθένειας Gravis, μιας αυτοάνοσης διαταραχής της νευρομυϊκής σύναψης.
Όταν τα AChR είναι αρνητικά αλλά τα συμπτώματα παραμένουν ύποπτα, ο έλεγχος επεκτείνεται σε αντισώματα MuSK, αντισώματα LRP4 και ηλεκτροφυσιολογικό έλεγχο.
Η εξέταση δεν ερμηνεύεται μόνη της. Το αποτέλεσμα πρέπει να συνδυάζεται με νευρολογική εκτίμηση, ιστορικό, κλινική εικόνα, ηλεκτρομυογράφημα και, όταν χρειάζεται, απεικόνιση θώρακος για έλεγχο θύμου αδένα.
1Τι είναι τα αντισώματα AChR;
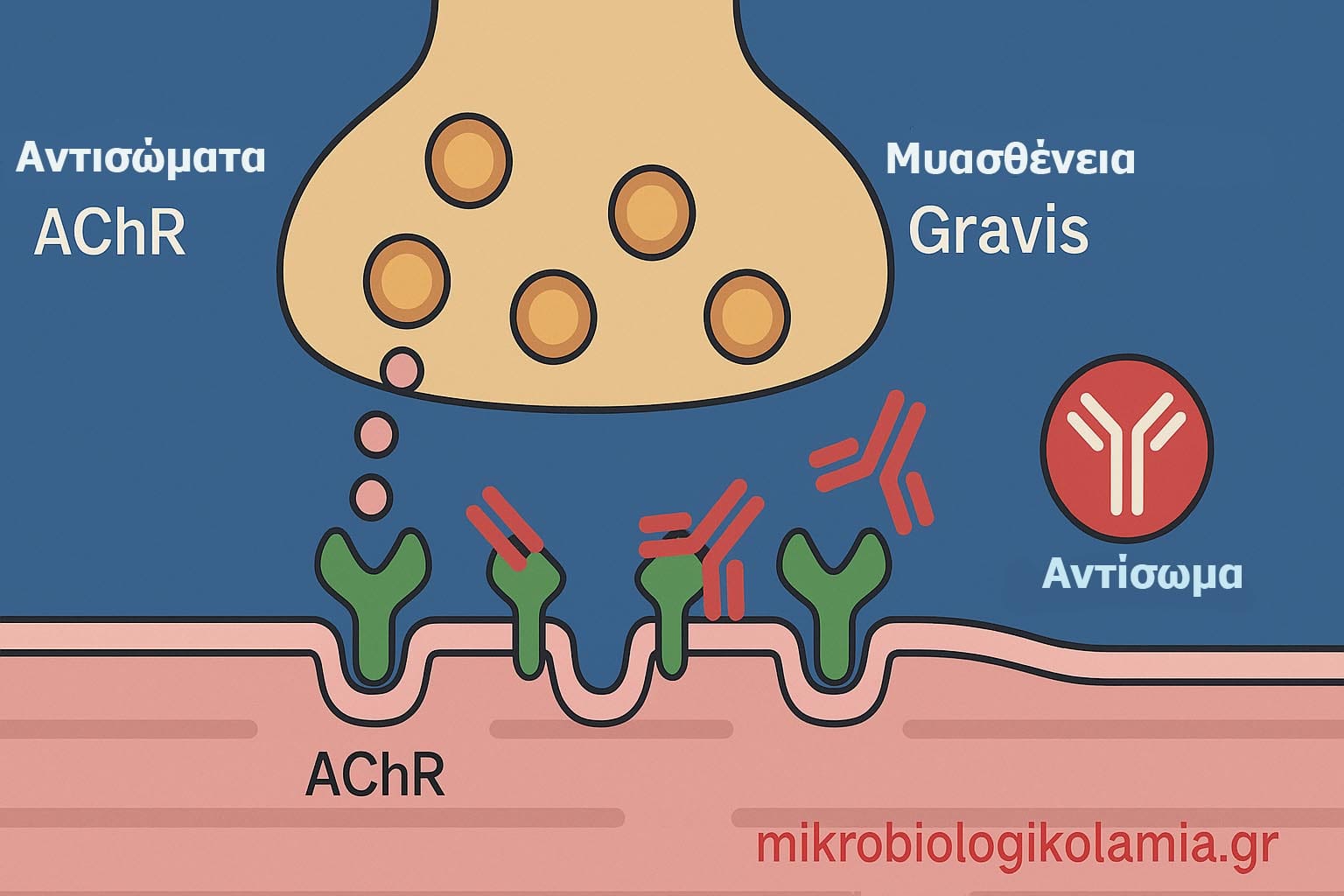
Τα αντισώματα AChR είναι αυτοαντισώματα που στρέφονται εναντίον του υποδοχέα της ακετυλοχολίνης στη νευρομυϊκή σύναψη. Η νευρομυϊκή σύναψη είναι το σημείο όπου το νεύρο μεταδίδει το σήμα στον μυ ώστε να γίνει σύσπαση. Για να λειτουργήσει σωστά αυτή η μετάδοση, η ακετυλοχολίνη απελευθερώνεται από το νεύρο και συνδέεται με ειδικούς υποδοχείς στην επιφάνεια του μυός.
Όταν υπάρχουν αντισώματα έναντι του AChR, η φυσιολογική αυτή επικοινωνία διαταράσσεται. Τα αντισώματα μπορεί να μπλοκάρουν τον υποδοχέα, να προκαλούν καταστροφή ή εσωτερίκευσή του ή να ενεργοποιούν ανοσολογικούς μηχανισμούς που μειώνουν τον αριθμό των λειτουργικών υποδοχέων. Το τελικό αποτέλεσμα είναι ότι ο μυς λαμβάνει ασθενέστερο σήμα από το νεύρο.
Η εξέταση για αντισώματα AChR χρησιμοποιείται κυρίως στη διερεύνηση της Μυασθένειας Gravis. Η θετικότητα των AChR αντισωμάτων αποτελεί ισχυρό εργαστηριακό στοιχείο υπέρ αυτοάνοσης μυασθένειας, ιδιαίτερα όταν ο ασθενής έχει τυπικά συμπτώματα όπως βλεφαρόπτωση, διπλωπία, κόπωση στην κατάποση, αλλαγή φωνής ή μυϊκή αδυναμία που χειροτερεύει με την προσπάθεια.
Η εξέταση όμως δεν είναι απλώς ένα «θετικό ή αρνητικό» αποτέλεσμα. Η αξία της εξαρτάται από το ιστορικό, την ηλικία, το είδος των συμπτωμάτων, τη διάρκεια της νόσου, την παρουσία ή όχι οφθαλμικής μορφής, τη μέθοδο μέτρησης και τον υπόλοιπο νευρολογικό έλεγχο.
Σε πρακτικό επίπεδο, η εξέταση απαντά σε ένα βασικό ερώτημα: υπάρχει ανοσολογική ένδειξη ότι το σώμα παράγει αντισώματα εναντίον της νευρομυϊκής σύναψης; Αν η απάντηση είναι ναι, η διαγνωστική πιθανότητα μυασθένειας αυξάνεται σημαντικά. Αν η απάντηση είναι όχι, η διερεύνηση μπορεί να συνεχιστεί με άλλα αντισώματα, όπως MuSK και LRP4, ή με ειδικές ηλεκτροφυσιολογικές εξετάσεις.
2Τι είναι η Μυασθένεια Gravis;
Η Μυασθένεια Gravis είναι χρόνια αυτοάνοση διαταραχή της νευρομυϊκής σύναψης. Η λέξη «μυασθένεια» περιγράφει τη μυϊκή αδυναμία, ενώ ο όρος «gravis» ιστορικά χρησιμοποιήθηκε επειδή η νόσος μπορεί να γίνει σοβαρή όταν προσβληθούν οι αναπνευστικοί ή βολβικοί μύες. Σήμερα, με έγκαιρη διάγνωση και κατάλληλη θεραπεία, η πρόγνωση είναι πολύ καλύτερη.
Το βασικό χαρακτηριστικό της νόσου είναι η κυμαινόμενη μυϊκή αδυναμία. Αυτό σημαίνει ότι τα συμπτώματα δεν είναι πάντα σταθερά. Ο ασθενής μπορεί να είναι σχετικά καλά το πρωί και να επιδεινώνεται το απόγευμα ή το βράδυ. Μπορεί επίσης να εμφανίζει αδυναμία μετά από επαναλαμβανόμενη χρήση ενός μυός και βελτίωση μετά από ανάπαυση.
Η νόσος μπορεί να εμφανιστεί με οφθαλμικά συμπτώματα, όπως βλεφαρόπτωση και διπλωπία, ή με γενικευμένη μορφή που επηρεάζει τους μύες του προσώπου, της κατάποσης, της ομιλίας, του αυχένα, των άκρων ή της αναπνοής. Σε ορισμένους ασθενείς η νόσος παραμένει καθαρά οφθαλμική, ενώ σε άλλους εξελίσσεται σε γενικευμένη.
Η Μυασθένεια Gravis δεν είναι τυπική μυοπάθεια. Ο μυς μπορεί να είναι δομικά φυσιολογικός, αλλά το σήμα που λαμβάνει από το νεύρο είναι ανεπαρκές. Αυτός είναι ο λόγος που εξετάσεις όπως η CK μπορεί να είναι φυσιολογικές, ενώ ο ασθενής έχει έντονη λειτουργική αδυναμία.
Στην αυτοάνοση μορφή, τα συχνότερα αντισώματα είναι τα AChR. Σε μικρότερο ποσοστό υπάρχουν MuSK ή LRP4 αντισώματα. Σε ορισμένους ασθενείς δεν ανιχνεύονται αντισώματα με τις διαθέσιμες μεθόδους, παρότι η κλινική και ηλεκτροφυσιολογική εικόνα παραμένει συμβατή με μυασθένεια.
3Πότε ζητείται η εξέταση;
Η εξέταση για αντισώματα AChR ζητείται όταν υπάρχει υποψία μυασθένειας gravis ή όταν χρειάζεται να διερευνηθεί ανεξήγητη μυϊκή αδυναμία που έχει χαρακτηριστικά νευρομυϊκής διαταραχής. Δεν ζητείται ως γενικός προληπτικός έλεγχος. Η αξία της είναι μεγαλύτερη όταν υπάρχει συγκεκριμένη κλινική υποψία.
Ο ιατρός μπορεί να τη ζητήσει σε ασθενή με βλεφαρόπτωση που αλλάζει μέσα στην ημέρα, διπλωπία που δεν εξηγείται από άλλη οφθαλμολογική ή νευρολογική αιτία, αδυναμία στη μάσηση, δυσκολία στην κατάποση, κόπωση στην ομιλία ή γενικευμένη μυϊκή αδυναμία που επιδεινώνεται με την προσπάθεια.
- Οφθαλμικά συμπτώματα: πτώση βλεφάρου, διπλωπία, κόπωση των ματιών, επιδείνωση προς το τέλος της ημέρας.
- Βολβικά συμπτώματα: δυσκολία στην κατάποση, πνιγμονή, ρινική φωνή, κόπωση στην ομιλία, δυσκολία στη μάσηση.
- Μυϊκή αδυναμία άκρων: δυσκολία σε σκάλες, σήκωμα χεριών, παρατεταμένη ορθοστασία ή καθημερινές κινήσεις που κουράζουν δυσανάλογα.
- Αναπνευστικά συμπτώματα: δύσπνοια, ορθόπνοια, αδυναμία αποτελεσματικού βήχα ή αίσθημα κόπωσης στην αναπνοή.
Η εξέταση μπορεί επίσης να ζητηθεί όταν υπάρχει ήδη διάγνωση μυασθένειας αλλά χρειάζεται ορολογική ταξινόμηση. Η διάκριση μεταξύ AChR-θετικής, MuSK-θετικής, LRP4-θετικής ή οροαρνητικής μυασθένειας μπορεί να επηρεάσει τη θεραπευτική στρατηγική, την πρόγνωση και την ανάγκη για επιπλέον έλεγχο.
Σε ασθενή με ύποπτη πρόσθια μεσοθωρακική μάζα ή θύμωμα, τα AChR αντισώματα μπορεί επίσης να ζητηθούν, επειδή η μυασθένεια σχετίζεται με παθήσεις του θύμου. Αντίστροφα, σε ασθενή με AChR-θετική μυασθένεια, συχνά χρειάζεται απεικόνιση θώρακος.
4AChR, MuSK και LRP4: ποια η διαφορά;
Τα AChR, MuSK και LRP4 είναι οι τρεις βασικοί ορολογικοί στόχοι στη σύγχρονη διάγνωση της αυτοάνοσης μυασθένειας. Όλοι σχετίζονται με τη νευρομυϊκή σύναψη, αλλά δεν αντιπροσωπεύουν την ίδια παθοφυσιολογία ούτε την ίδια κλινική εικόνα.
Τα AChR αντισώματα στρέφονται εναντίον του υποδοχέα της ακετυλοχολίνης. Είναι τα συχνότερα και συνδέονται συχνά με κλασική γενικευμένη μυασθένεια. Τα MuSK αντισώματα στρέφονται εναντίον μιας πρωτεΐνης που είναι απαραίτητη για την οργάνωση και διατήρηση της νευρομυϊκής σύναψης. Η MuSK-θετική μυασθένεια μπορεί να έχει έντονα βολβικά, προσωπικά ή αναπνευστικά συμπτώματα. Τα LRP4 αντισώματα αφορούν έναν υποδοχέα που συμμετέχει στην ενεργοποίηση του MuSK και ζητούνται κυρίως σε επιλεγμένες διπλά οροαρνητικές περιπτώσεις.
| Αντίσωμα | Στόχος | Πότε είναι χρήσιμο | Κλινική σημασία |
|---|---|---|---|
| AChR | Υποδοχέας ακετυλοχολίνης | Πρώτη εξέταση σε ύποπτη μυασθένεια | Συχνότερος δείκτης, ισχυρή διαγνωστική αξία |
| MuSK | Muscle-specific kinase | Όταν AChR είναι αρνητικά ή υπάρχει ύποπτη βολβική εικόνα | Μπορεί να σχετίζεται με πιο ιδιαίτερο θεραπευτικό προφίλ |
| LRP4 | LRP4, μέρος του συστήματος agrin-LRP4-MuSK | Σε επιλεγμένες AChR/MuSK αρνητικές περιπτώσεις | Χρήσιμο σε δύσκολες ή οροαρνητικές διαγνώσεις |
Στην πράξη, ο έλεγχος συχνά ξεκινά με AChR. Αν είναι αρνητικά και η κλινική υποψία παραμένει, ακολουθεί MuSK. Αν και αυτό είναι αρνητικό, μπορεί να εξεταστεί LRP4 ή πιο εξειδικευμένο πάνελ σε κέντρο νευροανοσολογίας. Η σειρά αυτή δεν είναι απόλυτη· εξαρτάται από το ιστορικό και τη διαθεσιμότητα των εξετάσεων.
5Τύποι AChR αντισωμάτων
Τα AChR αντισώματα μπορούν να χωριστούν σε επιμέρους κατηγορίες ανάλογα με τον τρόπο δράσης τους. Η διάκριση αυτή έχει περισσότερο εργαστηριακή και ειδική κλινική σημασία, αλλά βοηθά να κατανοηθεί γιατί η μυασθένεια μπορεί να έχει διαφορετική ένταση και μορφή από ασθενή σε ασθενή.
Binding αντισώματα: Είναι τα συχνότερα και συνήθως τα πρώτα που αναζητούνται. Συνδέονται με τον υποδοχέα της ακετυλοχολίνης και αποτελούν τον βασικό ορολογικό δείκτη της AChR-θετικής μυασθένειας. Σε πολλά εργαστήρια, όταν αναφέρεται «AChR antibodies», εννοούνται κυρίως τα binding αντισώματα.
Blocking αντισώματα: Παρεμποδίζουν λειτουργικά τη σύνδεση της ακετυλοχολίνης με τον υποδοχέα. Δεν ανιχνεύονται πάντα χωριστά στην καθημερινή πράξη, αλλά μπορεί να έχουν συμπληρωματική αξία σε επιλεγμένες περιπτώσεις.
Modulating αντισώματα: Προκαλούν μείωση του αριθμού των λειτουργικών υποδοχέων στην επιφάνεια του μυός, επειδή οδηγούν σε εσωτερίκευση ή αποδόμηση του υποδοχέα. Η παρουσία τους μπορεί να ενισχύσει τη διαγνωστική εικόνα όταν συνυπάρχει με άλλα ευρήματα.
Δεν χρειάζεται κάθε ασθενής να κάνει και τους τρεις υποτύπους. Ο νευρολόγος επιλέγει ποιος έλεγχος είναι απαραίτητος ανάλογα με το περιστατικό. Σε αρκετές περιπτώσεις, το AChR binding είναι αρκετό ως αρχικός έλεγχος. Σε δύσκολες περιπτώσεις, όμως, ο πιο εκτεταμένος έλεγχος μπορεί να αυξήσει τη διαγνωστική ευαισθησία.
6Συμπτώματα που οδηγούν στον έλεγχο
Η μυασθένεια μπορεί να είναι δύσκολη στη διάγνωση επειδή τα συμπτώματα αλλάζουν. Ο ασθενής μπορεί να εξεταστεί σε στιγμή που αισθάνεται καλύτερα, ενώ λίγες ώρες αργότερα να εμφανίζει εμφανή αδυναμία. Αυτή η διακύμανση είναι βασικό στοιχείο που πρέπει να αναζητείται στο ιστορικό.
Τα οφθαλμικά συμπτώματα είναι συχνή αρχική εκδήλωση. Η βλεφαρόπτωση μπορεί να είναι μονόπλευρη ή αμφοτερόπλευρη, να χειροτερεύει με την παρατεταμένη χρήση των ματιών και να βελτιώνεται με ανάπαυση. Η διπλωπία μπορεί να εμφανίζεται μόνο σε ορισμένες κατευθύνσεις βλέμματος ή στο τέλος της ημέρας.
Τα βολβικά συμπτώματα είναι ιδιαίτερα σημαντικά. Περιλαμβάνουν δυσκολία στην κατάποση, πνιγμονή, κόπωση στη μάσηση, ρινική φωνή, βραχνάδα ή αδυναμία καθαρής άρθρωσης. Αυτά τα συμπτώματα μπορεί να αυξάνουν τον κίνδυνο εισρόφησης και χρειάζονται προσοχή.
Η γενικευμένη αδυναμία μπορεί να αφορά τον αυχένα, τους ώμους, τους μηρούς ή τα άκρα. Ο ασθενής μπορεί να δυσκολεύεται να ανέβει σκάλες, να σηκωθεί από καρέκλα, να σηκώσει τα χέρια πάνω από το κεφάλι ή να κρατήσει αντικείμενα για ώρα. Η αδυναμία συχνά δεν συνοδεύεται από πόνο ή αισθητικές διαταραχές.
Τα αναπνευστικά συμπτώματα είναι η πιο επείγουσα πλευρά της νόσου. Δύσπνοια, ορθόπνοια, αδύναμος βήχας ή αίσθημα ότι ο ασθενής δεν μπορεί να πάρει βαθιά ανάσα απαιτούν άμεση ιατρική αξιολόγηση.
7Προετοιμασία και δείγμα
Η εξέταση για αντισώματα AChR γίνεται με απλή αιμοληψία. Συνήθως απαιτείται ορός αίματος. Δεν χρειάζεται νηστεία και ο ασθενής μπορεί να προσέλθει οποιαδήποτε ώρα, εκτός αν υπάρχει άλλη οδηγία από τον θεράποντα ιατρό ή το εργαστήριο.
Η λήψη φαρμάκων δεν πρέπει να διακόπτεται αυθαίρετα. Αν ο ασθενής λαμβάνει πυριδοστιγμίνη, κορτικοστεροειδή, ανοσοκατασταλτικά, IVIG, βιολογικούς παράγοντες ή έχει υποβληθεί πρόσφατα σε πλάσμαφαίρεση, πρέπει να ενημερώνει τον ιατρό και το εργαστήριο. Αυτές οι πληροφορίες βοηθούν στην ερμηνεία, ακόμα και αν δεν αλλάζουν απαραίτητα την ίδια τη διαδικασία της αιμοληψίας.
- Νηστεία: Δεν απαιτείται.
- Δείγμα: Ορός αίματος.
- Ώρα αιμοληψίας: Συνήθως χωρίς περιορισμό.
- Φάρμακα: Δεν διακόπτονται χωρίς ιατρική οδηγία.
- Χρόνος απάντησης: Εξαρτάται από τη μέθοδο και από το αν η εξέταση γίνεται τοπικά ή σε συνεργαζόμενο εξειδικευμένο εργαστήριο.
8Μεθοδολογία ανίχνευσης
Τα αντισώματα AChR, MuSK και LRP4 μπορούν να ανιχνευθούν με διαφορετικές ανοσολογικές τεχνικές. Η μέθοδος έχει σημασία επειδή επηρεάζει την ευαισθησία, την ειδικότητα, τις μονάδες μέτρησης και το όριο θετικότητας.
Η RIA θεωρείται κλασική μέθοδος με υψηλή διαγνωστική αξία, αλλά απαιτεί ειδικές υποδομές λόγω ραδιοϊσοτόπων. Η ELISA είναι πιο διαδεδομένη σε πολλά εργαστήρια και χρησιμοποιείται για πρακτική ανοσοενζυμική ανίχνευση. Η CLIA προσφέρει αυτοματοποίηση και συχνά ποσοτικό αποτέλεσμα με καλή αναπαραγωγιμότητα.
Τα cell-based assays έχουν ιδιαίτερη αξία σε δύσκολες περιπτώσεις. Σε αυτές τις μεθόδους, τα αντιγόνα παρουσιάζονται στην επιφάνεια κυττάρων με πιο φυσιολογική διαμόρφωση, κάτι που μπορεί να επιτρέψει την ανίχνευση αντισωμάτων που δεν φαίνονται με κλασικές τεχνικές. Δεν είναι απαραίτητα η πρώτη εξέταση για όλους, αλλά μπορεί να είναι χρήσιμα σε οροαρνητικούς ασθενείς με έντονη κλινική υποψία.
Ένα συχνό λάθος είναι η απευθείας σύγκριση αριθμητικών αποτελεσμάτων από διαφορετικά εργαστήρια. Αν ένα εργαστήριο αναφέρει IU/L και άλλο nmol/L, ή αν χρησιμοποιούνται διαφορετικές πλατφόρμες, η σύγκριση μπορεί να είναι παραπλανητική. Ο σωστός τρόπος είναι να αξιολογείται κάθε αποτέλεσμα με βάση τα όρια αναφοράς της συγκεκριμένης μεθόδου.
9Ερμηνεία αποτελεσμάτων
Η ερμηνεία των AChR αντισωμάτων γίνεται με βάση το όριο αναφοράς του εργαστηρίου. Τα αποτελέσματα μπορεί να αναφέρονται ως αρνητικά, οριακά ή θετικά, ή να δίνονται με αριθμητική τιμή. Η θετικότητα ενισχύει σημαντικά την πιθανότητα μυασθένειας, ιδιαίτερα όταν τα συμπτώματα είναι συμβατά.
Ένα αρνητικό αποτέλεσμα σημαίνει ότι δεν ανιχνεύθηκαν αντισώματα με τη συγκεκριμένη μέθοδο. Δεν σημαίνει ότι δεν υπάρχει μυασθένεια. Αυτό είναι ιδιαίτερα σημαντικό σε οφθαλμική μυασθένεια, σε πρώιμη νόσο ή σε ασθενείς που έχουν λάβει ανοσοθεραπεία.
Ένα οριακό αποτέλεσμα απαιτεί προσοχή. Μπορεί να είναι πρώιμη θετικότητα, μη ειδικό εύρημα ή τεχνικό/μεθοδολογικό ζήτημα. Σε τέτοιες περιπτώσεις η επανάληψη, η επιβεβαίωση με άλλη μέθοδο ή η αξιολόγηση σε ειδικό κέντρο μπορεί να είναι απαραίτητη.
Ένα θετικό αποτέλεσμα είναι ισχυρό στοιχείο υπέρ AChR-θετικής μυασθένειας, αλλά δεν αντικαθιστά την κλινική διάγνωση. Ο νευρολόγος θα αξιολογήσει αν τα συμπτώματα, η κατανομή της αδυναμίας και η πορεία ταιριάζουν με μυασθένεια ή αν χρειάζεται διαφορετική διερεύνηση.
| Αποτέλεσμα | Τι σημαίνει | Τι πρέπει να γίνει |
|---|---|---|
| Αρνητικό | Δεν ανιχνεύονται AChR αντισώματα με τη συγκεκριμένη μέθοδο. | Αν η υποψία παραμένει, έλεγχος MuSK, LRP4 και ηλεκτροφυσιολογία. |
| Οριακό | Αμφίβολη ή χαμηλή θετικότητα. | Επανάληψη, επιβεβαίωση ή cell-based assay σε ειδική περίπτωση. |
| Θετικό | Συμβατό με AChR-θετική μυασθένεια όταν ταιριάζει η κλινική εικόνα. | Νευρολογική εκτίμηση, έλεγχος θύμου και θεραπευτικός σχεδιασμός. |
Ο τίτλος δεν είναι πάντα δείκτης βαρύτητας. Ένας υψηλός τίτλος δεν σημαίνει υποχρεωτικά πιο βαριά νόσο, και ένας χαμηλότερος τίτλος δεν σημαίνει απαραίτητα ήπια συμπτώματα. Η μυασθένεια παρακολουθείται κυρίως κλινικά.
10Αρνητικό αποτέλεσμα με ύποπτα συμπτώματα
Το αρνητικό AChR αποτέλεσμα είναι συχνή πηγή σύγχυσης. Πολλοί ασθενείς θεωρούν ότι αρνητικά αντισώματα σημαίνουν ότι αποκλείστηκε οριστικά η μυασθένεια. Αυτό δεν είναι σωστό. Η μυασθένεια μπορεί να είναι AChR-αρνητική, ειδικά όταν αφορά μόνο τα μάτια ή όταν τα αντισώματα είναι χαμηλού τίτλου και δεν ανιχνεύονται με την αρχική μέθοδο.
Σε τέτοιες περιπτώσεις ο έλεγχος συνήθως συνεχίζεται με MuSK αντισώματα. Αν και αυτά είναι αρνητικά, μπορεί να εξεταστούν LRP4 αντισώματα, ιδίως όταν η κλινική εικόνα παραμένει πειστική. Παράλληλα, το single-fiber EMG μπορεί να δώσει σημαντικές πληροφορίες για τη νευρομυϊκή μετάδοση.
Υπάρχει επίσης η κατηγορία της οροαρνητικής μυασθένειας, όπου οι διαθέσιμες ορολογικές εξετάσεις είναι αρνητικές, αλλά η κλινική και ηλεκτροφυσιολογική εικόνα παραμένει συμβατή. Σε αυτές τις περιπτώσεις χρειάζεται εξειδικευμένη νευρολογική αξιολόγηση, γιατί πρέπει να αποκλειστούν και άλλες παθήσεις που μιμούνται τη μυασθένεια.
11Θετικό αποτέλεσμα: επόμενα βήματα
Ένα θετικό AChR αποτέλεσμα είναι σημαντικό εύρημα. Το επόμενο βήμα δεν είναι απλώς να «θεραπευτεί το αποτέλεσμα», αλλά να επιβεβαιωθεί η συνολική διάγνωση και να εκτιμηθεί η έκταση της νόσου. Ο νευρολόγος θα αξιολογήσει αν η νόσος είναι οφθαλμική ή γενικευμένη, αν υπάρχουν βολβικά ή αναπνευστικά συμπτώματα και αν χρειάζεται άμεση παρέμβαση.
Συνήθως ακολουθεί απεικόνιση θώρακος για έλεγχο του θύμου αδένα. Η παρουσία θύμωματος αλλάζει τη διαχείριση. Ακόμη και χωρίς θύμωμα, η σχέση AChR-θετικής μυασθένειας με τον θύμο καθιστά τον απεικονιστικό έλεγχο σημαντικό.
Η θεραπευτική προσέγγιση μπορεί να περιλαμβάνει συμπτωματική αγωγή, ανοσοτροποποιητική θεραπεία, κορτικοστεροειδή, ανοσοκατασταλτικά, βιολογικούς παράγοντες ή επείγουσες θεραπείες όπως IVIG και πλάσμαφαίρεση σε ειδικές περιπτώσεις. Η επιλογή δεν γίνεται από το εργαστηριακό αποτέλεσμα μόνο, αλλά από τη συνολική βαρύτητα και το προφίλ του ασθενούς.
- Νευρολογική εκτίμηση και καταγραφή βαρύτητας.
- Έλεγχος θύμου με αξονική ή μαγνητική θώρακος.
- Ηλεκτροφυσιολογικός έλεγχος αν χρειάζεται επιβεβαίωση.
- Έλεγχος θυρεοειδούς και άλλων συνοδών αυτοάνοσων νοσημάτων.
- Εξατομικευμένος θεραπευτικός σχεδιασμός.
12Συνοδευτικές εξετάσεις αίματος
Η μυασθένεια είναι αυτοάνοσο νόσημα και μπορεί να συνυπάρχει με άλλες αυτοάνοσες καταστάσεις. Για αυτό, πέρα από τα αντισώματα AChR, MuSK και LRP4, συχνά χρειάζεται ευρύτερος εργαστηριακός έλεγχος. Ο στόχος είναι διπλός: να υποστηριχθεί η διάγνωση και να εκτιμηθεί η γενική κατάσταση πριν από θεραπευτικές αποφάσεις.
- TSH, FT4, αντι-TPO, αντι-TG: Η αυτοάνοση θυρεοειδοπάθεια μπορεί να συνυπάρχει με μυασθένεια και να επηρεάζει συμπτώματα όπως κόπωση, αίσθημα παλμών ή αδυναμία.
- Γενική αίματος: Χρήσιμη για βασική εκτίμηση, αλλά και πριν ή κατά τη διάρκεια ανοσοκατασταλτικών θεραπειών.
- Ηπατικά ένζυμα και νεφρική λειτουργία: Σημαντικά σε θεραπευτικό σχεδιασμό και παρακολούθηση φαρμάκων.
- CRP και ΤΚΕ: Μπορούν να βοηθήσουν όταν υπάρχει υποψία φλεγμονώδους ή συστηματικής νόσου.
- ANA και ENA: Ζητούνται επιλεκτικά όταν υπάρχουν στοιχεία για άλλο συστηματικό αυτοάνοσο νόσημα.
- Βιταμίνη Β12, φυλλικό, φερριτίνη: Δεν διαγιγνώσκουν μυασθένεια, αλλά μπορεί να βοηθήσουν στη διερεύνηση κόπωσης ή νευρολογικών συμπτωμάτων.
Ο συνοδός εργαστηριακός έλεγχος δεν πρέπει να οδηγεί σε υπερδιάγνωση. Πρέπει να καθοδηγείται από τα συμπτώματα, το ιστορικό και το θεραπευτικό πλάνο. Σε έναν ασθενή που πρόκειται να λάβει ανοσοκατασταλτικά, ο προθεραπευτικός έλεγχος είναι διαφορετικός από έναν ασθενή που βρίσκεται σε αρχική διερεύνηση ήπιας οφθαλμικής μορφής.
13Ηλεκτροφυσιολογικός και απεικονιστικός έλεγχος
Ο ηλεκτροφυσιολογικός έλεγχος είναι ιδιαίτερα χρήσιμος όταν η διάγνωση δεν είναι ξεκάθαρη. Ελέγχει λειτουργικά τη νευρομυϊκή μετάδοση και μπορεί να επιβεβαιώσει ότι το πρόβλημα βρίσκεται στη σύναψη νεύρου-μυός.
Το repetitive nerve stimulation βασίζεται σε επαναλαμβανόμενα ηλεκτρικά ερεθίσματα και καταγράφει αν υπάρχει σταδιακή μείωση της μυϊκής απόκρισης. Η εξέταση είναι χρήσιμη κυρίως σε γενικευμένη μυασθένεια, αλλά μπορεί να είναι λιγότερο ευαίσθητη σε καθαρά οφθαλμική μορφή.
Το single-fiber EMG είναι πιο ευαίσθητη εξέταση για διαταραχή νευρομυϊκής μετάδοσης. Μετρά τη μεταβλητότητα στη μετάδοση μεταξύ νεύρου και μυϊκής ίνας. Είναι ιδιαίτερα χρήσιμο όταν τα αντισώματα είναι αρνητικά αλλά τα συμπτώματα παραμένουν τυπικά.
Ο απεικονιστικός έλεγχος αφορά κυρίως τον θύμο αδένα. Σε ασθενείς με AChR-θετική μυασθένεια, η αξονική ή μαγνητική θώρακος βοηθά στον έλεγχο για θύμωμα ή υπερπλασία θύμου. Η επιλογή της εξέτασης εξαρτάται από την ηλικία, το ιστορικό, την κλινική εικόνα και τη διαθεσιμότητα.
Σε άτυπα συμπτώματα, όπως αισθητικές διαταραχές, έντονος πόνος, μονόπλευρη πυραμιδική σημειολογία ή σημεία κεντρικού νευρικού συστήματος, μπορεί να χρειαστεί διαφορετική απεικόνιση, όπως MRI εγκεφάλου ή αυχενικής μοίρας, για αποκλεισμό άλλων αιτιών.
14Θύμωμα και θύμος αδένας
Ο θύμος αδένας έχει κεντρική θέση στην AChR-θετική μυασθένεια. Είναι όργανο του ανοσοποιητικού συστήματος που συμμετέχει στην ωρίμανση των Τ-λεμφοκυττάρων. Σε πολλούς ασθενείς με μυασθένεια παρατηρούνται αλλαγές στον θύμο, όπως υπερπλασία ή θύμωμα.
Το θύμωμα είναι όγκος του θύμου αδένα. Δεν σημαίνει ότι κάθε ασθενής με AChR αντισώματα έχει θύμωμα, αλλά η σχέση είναι αρκετά σημαντική ώστε ο έλεγχος του μεσοθωρακίου να αποτελεί συχνό βήμα μετά τη διάγνωση. Η απεικόνιση βοηθά να διαπιστωθεί αν υπάρχει μάζα και αν χρειάζεται θωρακοχειρουργική αξιολόγηση.
Η θυμεκτομή μπορεί να συζητηθεί σε συγκεκριμένους ασθενείς, ιδιαίτερα σε γενικευμένη AChR-θετική μυασθένεια ή όταν υπάρχει θύμωμα. Δεν αφορά όλους τους ασθενείς και η απόφαση λαμβάνεται από εξειδικευμένη ομάδα, με βάση την ηλικία, τη βαρύτητα, τη διάρκεια της νόσου και τα απεικονιστικά ευρήματα.
15Παιδιά, κύηση και νεογνική μυασθένεια
Η μυασθένεια στα παιδιά χρειάζεται ιδιαίτερη προσέγγιση, επειδή πρέπει να διακριθεί η αυτοάνοση νεανική μυασθένεια από τα συγγενή μυασθενικά σύνδρομα. Τα συγγενή σύνδρομα δεν προκαλούνται από αυτοαντισώματα και επομένως μπορεί να έχουν αρνητικό ορολογικό έλεγχο. Για αυτό η παιδιατρική νευρολογική εκτίμηση είναι απαραίτητη.
Στην κύηση, η μυασθένεια μπορεί να παραμείνει σταθερή, να βελτιωθεί ή να επιδεινωθεί. Η πορεία δεν είναι ίδια σε όλες τις γυναίκες. Τα AChR αντισώματα μπορούν να περάσουν τον πλακούντα και να προκαλέσουν παροδική νεογνική μυασθένεια. Το νεογνό μπορεί να εμφανίσει υποτονία, δυσκολία στη σίτιση, αδύναμο κλάμα ή αναπνευστική δυσκολία.
Η νεογνική μυασθένεια είναι συνήθως παροδική, επειδή τα μητρικά αντισώματα απομακρύνονται σταδιακά από την κυκλοφορία του νεογνού. Παρ’ όλα αυτά, χρειάζεται έγκαιρη αναγνώριση και παρακολούθηση από νεογνολόγο. Η προγεννητική ενημέρωση της μαιευτικής και νεογνολογικής ομάδας είναι σημαντική.
Στην κύηση και στον τοκετό χρειάζεται προσοχή στα φάρμακα, στην αναισθησία και στη διαχείριση πιθανής επιδείνωσης. Η γυναίκα με μυασθένεια πρέπει να παρακολουθείται από νευρολόγο και μαιευτήρα με εμπειρία σε νευρολογικά νοσήματα της κύησης.
16Φάρμακα που επιδεινώνουν τη μυασθένεια
Ορισμένα φάρμακα μπορούν να επιδεινώσουν τη μυασθένεια επειδή επηρεάζουν τη νευρομυϊκή μετάδοση. Αυτό δεν σημαίνει ότι κάθε τέτοιο φάρμακο απαγορεύεται σε κάθε ασθενή. Σημαίνει όμως ότι χρειάζεται προσοχή, ενημέρωση του ιατρού και εκτίμηση κινδύνου-οφέλους.
- Αμινογλυκοσίδες: Μπορούν να επηρεάσουν σημαντικά τη νευρομυϊκή μετάδοση.
- Φθοριοκινολόνες: Έχουν αναφερθεί επιδεινώσεις σε ασθενείς με μυασθένεια.
- Μακρολίδες: Μπορεί να επιδεινώσουν συμπτώματα σε ευαίσθητους ασθενείς.
- Μαγνήσιο: Ιδιαίτερη προσοχή σε ενδοφλέβια χορήγηση ή υψηλές δόσεις.
- Β-αναστολείς: Μπορεί να αυξήσουν την κόπωση ή την αδυναμία.
- Νευρομυϊκοί αποκλειστές: Χρειάζονται προσοχή σε χειρουργείο και αναισθησία.
Ο ασθενής με γνωστή μυασθένεια πρέπει να ενημερώνει κάθε ιατρό, οδοντίατρο ή αναισθησιολόγο για τη διάγνωση. Αυτό είναι ιδιαίτερα σημαντικό πριν από χειρουργική επέμβαση, χορήγηση αντιβιοτικών ή ενδοφλέβια φαρμακευτική αγωγή.
17Παρακολούθηση μετά τη διάγνωση
Η παρακολούθηση της μυασθένειας είναι κυρίως κλινική. Ο νευρολόγος αξιολογεί τη μυϊκή ισχύ, την κόπωση, την οφθαλμική συμμετοχή, την κατάποση, την ομιλία, την αναπνοή και την ανταπόκριση στη θεραπεία. Οι εργαστηριακές εξετάσεις βοηθούν, αλλά δεν αντικαθιστούν την κλινική εκτίμηση.
Ο τίτλος των AChR αντισωμάτων δεν χρειάζεται να μετριέται σε κάθε επίσκεψη. Σε ορισμένους ασθενείς μπορεί να μειώνεται με τη θεραπεία, αλλά η σχέση τίτλου και συμπτωμάτων δεν είναι πάντα γραμμική. Έτσι, ένας ασθενής μπορεί να βελτιώνεται κλινικά χωρίς εντυπωσιακή μεταβολή του τίτλου ή να έχει μεταβολές στον τίτλο χωρίς αντίστοιχη αλλαγή συμπτωμάτων.
Σε ασθενείς που λαμβάνουν κορτικοστεροειδή ή ανοσοκατασταλτικά, η παρακολούθηση περιλαμβάνει συχνά γενική αίματος, ηπατικά ένζυμα, νεφρική λειτουργία, γλυκόζη, λιπίδια ή άλλες εξετάσεις ανάλογα με την αγωγή. Στόχος είναι η ισορροπία ανάμεσα στον έλεγχο της νόσου και στην αποφυγή ανεπιθύμητων ενεργειών.
Η καταγραφή συμπτωμάτων από τον ίδιο τον ασθενή μπορεί να βοηθήσει. Για παράδειγμα, πότε εμφανίζεται βλεφαρόπτωση, αν υπάρχει δυσκολία στη μάσηση στο τέλος του γεύματος, αν η φωνή αλλάζει μετά από ομιλία ή αν η κόπωση επηρεάζει την καθημερινότητα. Αυτές οι πληροφορίες είναι συχνά πιο χρήσιμες από μία μεμονωμένη τιμή αντισωμάτων.
18Συχνές παγίδες στην ερμηνεία
Η πρώτη παγίδα είναι η υπερερμηνεία ενός θετικού αποτελέσματος χωρίς συμβατή κλινική εικόνα. Αν και τα AChR αντισώματα έχουν μεγάλη διαγνωστική αξία, κάθε εργαστηριακό αποτέλεσμα πρέπει να ερμηνεύεται μέσα στο σωστό κλινικό πλαίσιο.
Η δεύτερη παγίδα είναι η υποτίμηση ενός αρνητικού αποτελέσματος. Αρνητικά AChR δεν αποκλείουν μυασθένεια. Η νόσος μπορεί να είναι MuSK-θετική, LRP4-θετική ή οροαρνητική. Αυτό ισχύει ιδιαίτερα σε οφθαλμική μορφή ή σε ασθενείς που εξετάζονται νωρίς στην πορεία της νόσου.
Η τρίτη παγίδα είναι η σύγκριση αποτελεσμάτων διαφορετικών εργαστηρίων. Αν αλλάξει η μέθοδος, αλλάζει και το cut-off. Για παρακολούθηση τάσης, είναι προτιμότερο να χρησιμοποιείται το ίδιο εργαστήριο ή τουλάχιστον η ίδια μέθοδος, όταν αυτό είναι πρακτικά εφικτό.
Η τέταρτη παγίδα είναι η παραγνώριση φαρμάκων που επιδεινώνουν τη μυασθένεια. Ένας ασθενής μπορεί να φαίνεται ότι «χειροτερεύει η νόσος», ενώ στην πραγματικότητα έχει λάβει φάρμακο που επιβαρύνει τη νευρομυϊκή μετάδοση.
Η πέμπτη παγίδα είναι η σύγχυση με άλλες παθήσεις. Η διπλωπία, η κόπωση, η αδυναμία ή η δυσφαγία μπορεί να έχουν πολλές αιτίες. Θυρεοειδική οφθαλμοπάθεια, εγκεφαλικά επεισόδια, μυοπάθειες, παθήσεις κινητικού νευρώνα, περιφερικές νευροπάθειες και σύνδρομο Lambert-Eaton μπορεί να μπουν στη διαφορική διάγνωση.
19Πότε χρειάζεται άμεση ιατρική εκτίμηση;
Η μυασθένεια μπορεί να είναι ήπια, αλλά μπορεί και να επιδεινωθεί γρήγορα. Η αναπνευστική και βολβική συμμετοχή είναι οι πιο σημαντικές καταστάσεις που δεν πρέπει να καθυστερούν. Ο ασθενής πρέπει να αναζητήσει άμεση ιατρική εκτίμηση όταν εμφανίζεται δύσπνοια, δυσκολία στην κατάποση ή ταχεία επιδείνωση της αδυναμίας.
- Δύσπνοια, ορθόπνοια ή αίσθημα ότι η αναπνοή κουράζει.
- Αδυναμία κατάποσης υγρών ή τροφής.
- Πνιγμονή, βήχας κατά το φαγητό ή εισρόφηση.
- Αδυναμία να κρατηθεί το κεφάλι.
- Ταχεία επιδείνωση φωνής, ομιλίας ή μάσησης.
- Νέα σοβαρή αδυναμία μετά από λοίμωξη, χειρουργείο ή νέο φάρμακο.
20Συχνές ερωτήσεις
Χρειάζεται νηστεία για τα αντισώματα AChR;
Όχι, η εξέταση γίνεται με απλή αιμοληψία και δεν απαιτεί νηστεία.
Αν τα AChR είναι αρνητικά, αποκλείεται η μυασθένεια;
Όχι, γιατί μπορεί να υπάρχει AChR-αρνητική, MuSK-θετική, LRP4-θετική ή οροαρνητική μυασθένεια.
Τι σημαίνει θετικό AChR αποτέλεσμα;
Σημαίνει ότι ανιχνεύθηκαν αντισώματα συμβατά με αυτοάνοση μυασθένεια, εφόσον ταιριάζει η κλινική εικόνα.
Πρέπει να ελέγξω MuSK και LRP4 μαζί με AChR;
Ο έλεγχος MuSK και LRP4 είναι ιδιαίτερα χρήσιμος όταν τα AChR είναι αρνητικά αλλά η κλινική υποψία παραμένει.
Ο τίτλος των AChR δείχνει πόσο βαριά είναι η νόσος;
Όχι πάντα, γιατί η βαρύτητα της μυασθένειας εκτιμάται κυρίως κλινικά και όχι μόνο από τον αριθμό των αντισωμάτων.
Μπορεί η θεραπεία να επηρεάσει τα αποτελέσματα;
Ναι, θεραπείες όπως IVIG, πλάσμαφαίρεση, rituximab και ανοσοκαταστολή μπορεί να επηρεάσουν τους τίτλους αντισωμάτων.
Θετικά AChR σημαίνουν ότι έχω θύμωμα;
Όχι, αλλά σε AChR-θετική μυασθένεια συχνά συζητείται απεικονιστικός έλεγχος θώρακος για αξιολόγηση του θύμου.
21Τι να θυμάστε
Τα αντισώματα AChR είναι η βασική εξέταση αίματος για τη διερεύνηση της μυασθένειας gravis. Η θετικότητά τους έχει μεγάλη διαγνωστική αξία, αλλά το αποτέλεσμα πρέπει να ερμηνεύεται πάντα σε συνδυασμό με τα συμπτώματα και τη νευρολογική εξέταση.
Αρνητικά AChR δεν αποκλείουν τη μυασθένεια. Αν η κλινική εικόνα είναι τυπική, ο έλεγχος μπορεί να συνεχιστεί με MuSK, LRP4, cell-based assay ή ηλεκτροφυσιολογικές εξετάσεις όπως single-fiber EMG.
Ένα θετικό αποτέλεσμα συχνά οδηγεί σε πιο οργανωμένο έλεγχο: νευρολογική εκτίμηση, πιθανή απεικόνιση θώρακος για θύμο, έλεγχο συνοδών αυτοάνοσων νοσημάτων και θεραπευτικό σχεδιασμό. Η μυασθένεια είναι χρόνια νόσος, αλλά με σωστή διάγνωση και παρακολούθηση μπορεί να ελεγχθεί αποτελεσματικά.
Η πιο σημαντική πρακτική συμβουλή είναι να μη βασίζεται κανείς σε μία μόνο τιμή. Η μυασθένεια είναι νόσος που φαίνεται στο ιστορικό, στην κλινική εξέταση, στη λειτουργική κόπωση και στη συνολική εικόνα του ασθενούς. Τα αντισώματα είναι πολύτιμο εργαλείο, όχι απομονωμένη διάγνωση.
22Κλείστε εξέταση & Βιβλιογραφία
Ερμηνεία αποτελεσμάτων από ιατρό στο εργαστήριό μας. Μπορείτε να προγραμματίσετε εξέταση ή να δείτε τον πλήρη κατάλογο διαθέσιμων εξετάσεων.
Βιβλιογραφία & Πηγές
https://pmc.ncbi.nlm.nih.gov/articles/PMC7884987/
https://mikrobiologikolamia.gr/katalogos-eksetaseon/
Δρ. Παντελής Αναγνωστόπουλος
Μικροβιολογικό Εργαστήριο Λαμίας
Έσλιν 19, Λαμία 35100 • Τηλ. +30-22310-66841 • Δευτέρα–Παρασκευή 07:00–13:30